骨髄異形成症候 MDS 東京血液疾患診療所 MDS解析セット(OgataScore)

MDS解析セット(OgataScore)
フローサイトメトリー法によるMDSの解析が日本でも注目され始めました
Ogata Scoreはその名のとおりDr.Ogataが開発し2010年頃から欧米を中心に多くの施設で使用されてきたMDSの診断のための解析方法です。みなさん、診断の際にフローサイトメトリー検査をされたと思いますが、それはいわゆる「白血病解析セット」と言われるもので、白血病の診断に使用されるもので、特に芽球の少ないMDSの場合、ほとんど役に立ちません。
MDSの誤診で多いパターンが、良性疾患を低リスクMDSと間違えるというものです。
MDSのFCM解析の意義について、Dr.Ogataの講演から一部を抜粋します。
MDS 解析における FCM の意義

MDS は骨髄細胞に由来する悪性の病気で、頻度の高い疾患です。
骨髄の中では悪性化した造血細胞が増え、血液検査では貧血、血 小板減少、白血球減少(白血球の中でも好中球が減少)などの血球減少を認めます。
診断には、1)血球減少がある、2)骨髄検査で造血細胞に形の異常がある(異形成の確認)、3)血球減少を起こす他の疾患が除外 できる、の 3 つの条件を満たすことが必要です。しかしながら、異形成の確認と他の疾患の除外は、簡単ではないことが多く、しばし
ば診断に苦慮します。
WHO 分類では、MDS の診断補助のためフローサイトメトリーを用いた解析が推奨されています。MDS の骨髄細胞から診断に有用な 情報を得るためには、解析法に工夫が必要であり、いくつかの解析プロトコールが提案されています。それらの中でも、Ogata protocol(Ogata score)と呼ばれる解析法は、簡便で再現性が高いため、欧米を中心に多くの施設で使用されています。
参考文献
1. Valent P, Horny HP, Bennett JM, et al. Definitions and standards in
the diagnosis and treatment of the myelodysplastic syndromes: consensus
statements and report from a working conference. Leuk Res 31, 727-736,
2007
2. Hasserjian RP, Orazi A, Brunning RD, et al. Myelodysplastic syndromes:
overview. In WHO Classification of Tumours of Haematopoietic and Lymphoid
Tissues. 4th Edition. 2017. Edited by Swerdlow SH, Campo E, Harris NL,
et al.
3. Ogata K, Della Porta MG, Malcovati L, et al. Diagnostic utility of flow
cytometry in low-risk myelodysplastic syndromes: a prospective validation
study. Haematologica 94, 1066-1074, 2009
4. Porwit A, van de Loosdrecht AA, Bettelheim P, et al. Revisiting guidelines for integration of flow cytometry results in the WHO classification of myelodysplastic syndromes-proposal from the International/European LeukemiaNet Working Group for Flow Cytometry in MDS. Leukemia. 28, 1793-1798, 2014
Ogata protocol(Ogata score)の概要
MDS と良性疾患との鑑別を目的にしたフローサイトメトリー(FCM)解析法です。 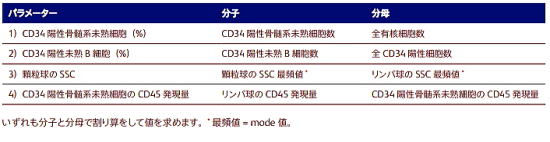 |
Ogata protocol(Ogata score)の解析方法
① 3 × 105 個の細胞を CD34, CD45, CD19 で染色し、フローサイトメーターで十分な数の有核細胞の情報を保存します(有核細胞数
10 万個以上を目標にします)。 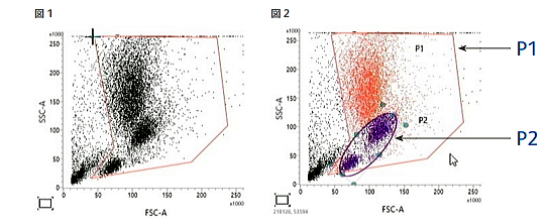 |
|
③ 図 3 : P2 の細胞を CD45 とCD34 で展開し、CD34 陽性細胞をゲーティングします(P3)。 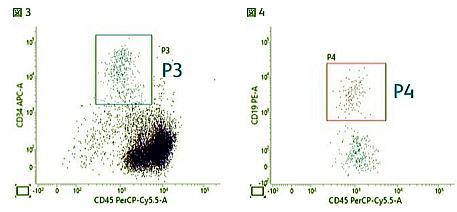
|
| ⑤ P3 細胞を CD34 とSSC で展開します。P4 細胞は左下方に集団をつくります。 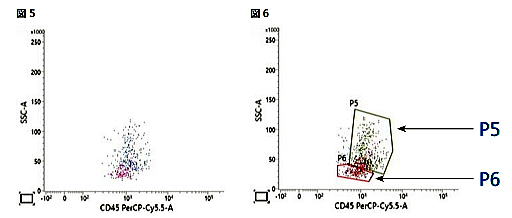 |
| ⑦P1 細胞を CD45 とSSC で展開し、顆粒球(P8)とリンパ球(P7)をゲーティングします。 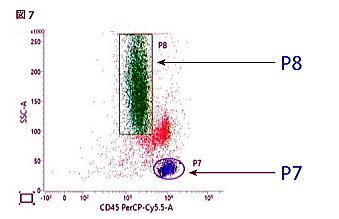 |
| ⑦ 図 8 : 顆粒球(P8)とリンパ球(P7)の SSC の最頻値(mode 値)を求めます。 図 9 : CD34 陽性骨髄系未熟細胞(P5)とリンパ球(P7)の CD45 発現量の平均値(GeoMean)を求めます。 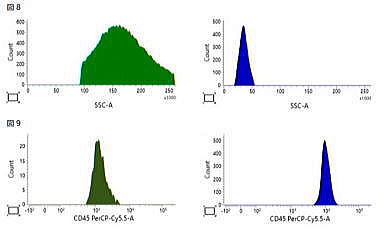 |
| 以上で得た情報から、4 つのパラメーター値を算出します。  |
|
CD34 陽性未熟 B 細胞の少ない検体について 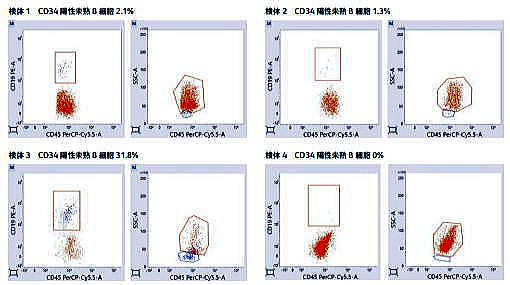 参考文献 |
結果の客観性 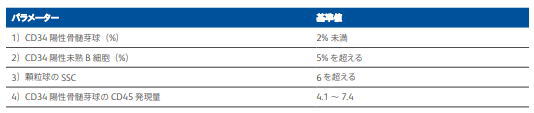 4つのパラメーター中2つ以上が異常値を示す場合、MDSなどの骨髄系腫瘍の可能性が非常に高いと考えられます。1つのパラメーター のみが異常の場合については、CD34 陽性骨髄芽球(%)、あるいは顆粒球の SSC が基準値を大きく逸脱している場合は、やはり MDS などの可能性が高いと考えられています。MDS であっても、これら 4 つのパラメーターに異常がない場合もありますので、この 点には留意して下さい。 参考文献 |
 |
| Ogata Protocolの共同研究者であるヨーロピアン・リューケミア・ネット(ELN)の面々と 2013年ドイツのミュンヘンにて  |



