骨髄異形成症候群 MDS 東京血液疾患診療所 骨髄異形成症候群とは

骨髄異形成症候群(MDS)とは

骨髄異形成症候群とは
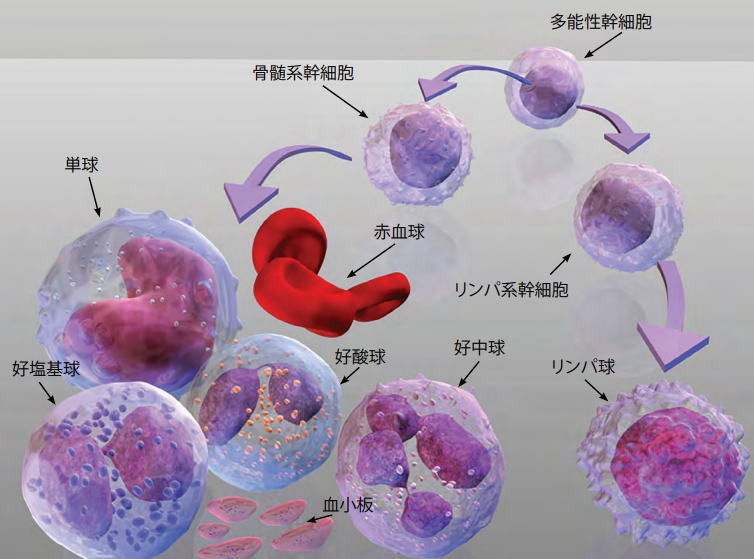
*骨髄で血液細胞を生み出す細胞(造血幹細胞)に異常が生じて形がいびつな血液細胞が作られること(異形成)と、 正常な血液細胞(赤血球、白血球、血小板)の数が減少することを特徴とする病気です。
| 赤血球が減少すると… ⇒貧血、めまい、だるさ、動悸、息切れなどの症状が出る 白血球が減少すると… ⇒感染が起こりやすくなり、発熱を伴う 血小板が減少すると… ⇒血が止まりにくくなる、出血しやすくなる |
*このような症状がみられますが、症状の程度は患者さんによってさまざまです。また、骨髄異形成症候群の中でも病型が分かれており、同じ病型であっても病気の進行具合、治療の効果などが大きく異なる場合があることがわかっています。
* 骨髄異形成症候群の影響により細胞の分化能が低下していった場合、正常な血液細胞が作られにくくなり、未熟な血液細胞(芽球)が増加していきます。
*高リスク群の骨髄異形成症候群の患者さんのおよそ3割が経過中に芽球が20%を超える場合があります。これを急性骨髄性白血病になったというときがありますが、芽球の性質が急性骨髄性白血病と同じになる訳ではありません。
参照⇒Living with MDS Lecture1 骨髄異形成症候群の診断 ②芽球が多い場合(YouTube)
骨髄異形成症候群(MDS)の発症
*造血幹細胞が腫瘍化して骨髄異形成症候群が発症するとされていますが、明確な発症原因がない骨髄異形成症候群が多数を占めています。
* 最近では、肺がん、リンパ腫などの治療や骨髄移植など(抗がん剤、放射線)により幹細胞が傷ついてしまい、 治療後5年前後で発症する治療由来性(二次性)の骨髄異形成症候群が10%程度確認されています。
| 全症例中の約10%が治療関連(二次性)の骨髄異形成症候群とされており、肺がんや 悪性リンパ腫、移植などの治療後の例が多くみられています。 |
*骨髄異形成症候群は高齢者に好発し、診断時の平均年齢は70歳前後となっています。
欧州の発症頻度:70歳以上の年齢層10万人当たり 20~50人/年
米国の発症頻度:65歳以上の年齢層10万人当たり 75人/年
*高齢化が進んでいる日本で米国の発症頻度を適用すると毎年2万人以上の骨髄異形成症候群患者が新たに発症していることとなり、現存する患者数は10万人をゆうにこえるであろうと予想されます。
骨髄異形成症候群(MDS)の病型
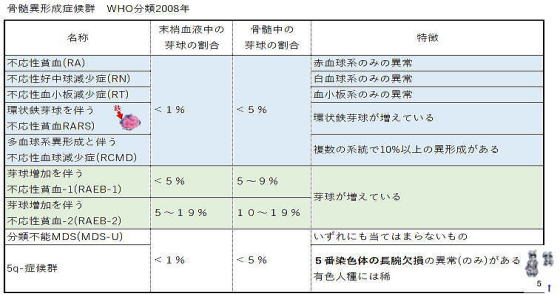
*骨髄異形成症候群は、骨髄中の芽球の割合(芽球にはリンパ芽球と骨髄芽球があり、骨髄異形成症候群で増えるものは骨髄芽球です)、末梢血の芽球の割合、異形成の程度などによって、いくつかの病型に分けられています。
| 分類の見方 *芽球……骨髄に未熟な細胞がどれぐらい存在しているか ⇒5%を超えると芽球の多い骨髄異形成症候群に分類されます。 20%以上は急性骨髄性白 血病(注1)と診断され、 5%未満の場合は環状鉄芽球、形態異常の状況で病型を決定します。 *環状鉄芽球……赤血球を作る赤芽球と呼ばれる細胞に見られる異常 ⇒15%未満or以上を確認し、さらに形態異常の状況で分類を判断します。 *形態異常……顕微鏡で確認できる細胞の形の異常 ⇒赤血球系、顆粒球系、巨核球のいずれかあるいは複数の細胞系統に 形態異常が発生しているかを確認します。 |
※芽球が少なく、骨髄細胞の染色体検査で問題がない場合、骨髄異形成症候群の診断が難しい場合がしばしばあります。
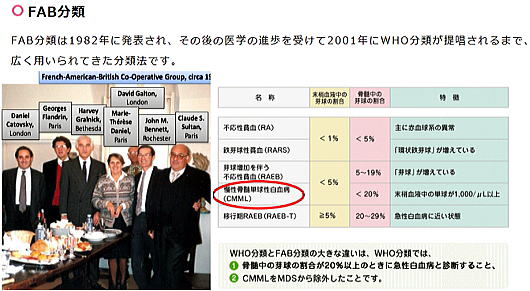
FAB分類を元に、2000年WHO分類が発表され、以降2年毎に更新されています。
どんどん無駄に複雑化していますので、ここには2008年版をのせておきます。
CMMLは一旦はMDSの分類から外されますが、後にMDS/MPNとして復活(?)しています。
*骨髄異形成/骨髄増殖性腫瘍(MDS/MPN)とは、異形成と増殖性の両方の特徴を有していますが、骨髄異形成症候群(MDS)または慢性骨髄増殖性疾患(CMPD)として適切に分類されないクローン性の骨髄性疾患です。
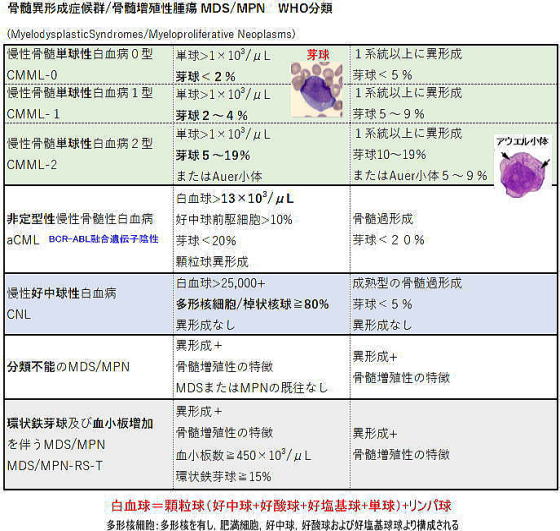
*MDS/MPNは大きく以下の3つのタイプに分類されます:
・単球が増えるタイプ ・好中球が増えるタイプ ・血小板や環状鉄芽球が増えるタイプ
骨髄異形成症候群(MDS)と診断されたら
*診断が確実か
血球減少で血液内科を受診した場合、血球減少を起こすさまざまな病気の中のどれであるかを見分け、原因は何かを調べます。
血液検査だけで原因がわかる病気(溶血性貧血など)もありますが、わからなかった場合、骨髄検査も行います。
骨髄検査の結果、染色体異常がある、環状鉄芽球がある、芽球が増加しているといった結果であれば、 骨髄異形成症候群の診断が比較的容易であるといわれています。 しかし、検査で明確な判断要素が見られない場合も多く、結果が不明確な場合もあります。このような場合、血液内科の専門医でも診断が難しいと言われています。
⇒その結果、骨髄異形成症候群と誤診される可能性があります。
骨髄異形成症候群と診断された患者の中で、10%以上は誤診であると考えられています。
骨髄異形成症候群の診断に精通している医師が極めて少ないため、血液内科のある大病院でも誤診は避けられません。骨髄異形成症候群の診断は、専門の医師に確実に行ってもらうことが望ましいです。
●現在、骨髄異形成症候群の診断には専門的な技術や知識が求められ、血液内科医であっても必ず骨髄異形成症候群について詳しいとは限りません。 診断が確実であっても 骨髄異形成症候群(MDS)の診断が正しい場合でも、現実的な問題として、
・外来で骨髄異形成症候群について説明する時間がない場合が多い
・医師自身に骨髄異形成症候群の十分な知識がない場合が多い
といった現状があります
よくある医師の説明 「いずれは白血病になる病気です」 「完治には骨髄移植しかありません」 「移植しかありませんが、あなたの年齢では無理です」 ... etc 医師に骨髄異形成症候群の知識がない場合、治療について移植の話ばかりされるなど、適切でない説明をされてしまうケースがしばしばあります。
骨髄異形成症候群(MDS)のリスク分類と予後
骨髄異形成症候群では、病気の経過(予後)を予測するために、国際予後判定システム(International Prognostic Scoring System:IPSS)というものがあります。 各項目(予後因子)の点数については、低いほど良い状態となり、3項目の点数の合計でリスク分類を行います。 なお、現在はIPSSを改訂して作成された、IPSS-Rというより詳細な分類があります。
リスク分類によって、ある程度予後を予測することができます。
Point ポイント ●リスク分類によって、ある程度予後を予測できますが、発表されているデータは治療法がなかった時代のものであることに注意が必要です。
参考動画:骨髄異形成症候群と診断されたら(Youtube) 次ページ:骨髄異形成症候群(MDS)のFCM検査


